服务热线
86-21-54488867 / 400-0534316
T/BHES 0001-2023 水质 碱度、碳酸盐和重碳酸盐的测定 自动电位滴定法
范围
本文件规定了自动电位滴定法测定水中碱度(总碱度、碳酸盐碱度、重碳酸盐碱度)和重碳酸盐、碳酸盐含量的方法。
本文件适用于地表水、地下水、大气降水、生活饮用水、污废水中碱度和重碳酸盐、碳酸盐含量的检测。
术语和定义
下列术语和定义适用于本文件。
碱度 alkalinity
碱性化合物能与氢离子(H+)结合,消耗酸标准溶液的能力称为水的碱度。碱度一般包括氢氧化钠碱度、碳酸盐碱度和重碳酸盐碱度。
滴定终点 titration endpoint
水样使用盐酸标准滴定溶液滴定,pH值到达预设值时即达到滴定终点。
方法原理
水样用盐酸标准滴定溶液滴定至规定的pH值,其终点用pH电极来指示。pH值为8.3时,水中氢氧根离子(OH-)已被中和,碳酸盐(CO32-)均变为重碳酸盐(HCO3-);继续滴定至pH值为4.4时,水中重碳酸盐(包括原有的和由碳酸盐转化成的)已被中和。根据上述两个终点到达时所消耗的盐酸标准滴定溶液的量,计算出水中的碱度、碳酸盐和重碳酸盐含量。
pH=8.3时,化学反应式:
OH-+H+=H2O
CO32-+H+=HCO3-
pH=4.4时,化学反应式:
HCO3-+H+=H2O+CO2
试剂和材料
除非另有说明,分析时均使用符合国家标准的分析纯试剂。
无二氧化碳水。
用于制备标准溶液及稀释用的蒸馏水或去离子水,临用前煮沸15min,冷却至室温。pH值应大于6.0,电导率小于0.2μs/cm。
碳酸钠(Na2CO3):优级纯。
邻苯二甲酸氢钾(KHC8H4O4)。
磷酸二氢钾(KH2PO4)。
磷酸氢二钠(Na2HPO4)。
硼砂(Na2B4O7·10H2O)。
浓盐酸(ρ=1.19g/mL)。
碳酸钠基准溶液:c(1/2 Na2CO3)=0.0250mol/L。
称取1.3249g(于180°C烘干2h)的基准无水碳酸钠(Na2CO3)溶于少量无二氧化碳水,移入1L容量瓶中,用水稀释至标线,摇匀。贮存于聚乙烯瓶中,保存时间不超过1周。
盐酸标准滴定溶液:c(HCl)=0.0250mol/L。
配制:用分度吸量管吸取2.1mL浓盐酸,用水稀释至1L,此溶液浓度约为0.0250mol/L。
标定:用单标线移液管吸取15.00mL碳酸钠基准溶液于测量杯中,加水稀释至约50mL,用盐酸标准滴定溶液滴定至pH为4.4,记录盐酸标准滴定溶液用量,按公式(1)计算其准确浓度:![]()
式中:
C——盐酸标准滴定溶液浓度,单位为摩尔每升(mol/L);
V——盐酸标准滴定溶液用量,单位为毫升(mL)。
pH标准缓冲溶液
pH标准缓冲溶液(pH=4.00,25°C),c(KHC8H4O4)=0.05mol/L。
称取事先在110~120°C干燥2~3h的邻苯二甲酸氢钾10.12g,溶于水,移入1L容量瓶中,稀释至标线,摇匀。
pH标准缓冲溶液(pH=6.86,25°C),c(KH2PO4)=0.025mol/L,c(Na2HPO4)=0.025mol/L。
称取事先在110~120°C干燥(2~3)h的磷酸二氢钾3.388g和磷酸氢二钠3.533g,溶于水,移入1L容量瓶中,稀释至标线,摇匀。
pH标准缓冲溶液(pH=9.18,25°C),c(Na2B4O7)=0.01mol/L。
为了使晶体具有一定的组成,应称取与饱和溴化钠(或氯化钠加蔗糖)溶液(室温)共同放置在干燥器中平衡48h的硼砂3.80g,溶于水,移入1L容量瓶中,稀释至标线,摇匀。
注1:标准缓冲溶液一般是在聚乙烯瓶中密闭保存。在4°C以下冷藏可保存2~72个月,当发现有浑浊、发霉或沉淀现象时,不能继续使用。
注2:可购买市售合格标准缓冲溶液,按说明书使用。
仪器和设备
自动电位滴定仪:电位范围−1000 mV~1000 mV,电位分辨率0.1mV。计量性能应符合 JJG 814 关于0.5级以上自动电位滴定仪的相关规定。
pH电极。
滴定管:20mL,容量允差应符合 JJG 814 关于0.5级以上自动电位滴定仪的相关规定。
测量杯:容积不小于150mL。
搅拌器。
一般实验室常用器皿和设备。
样品
一般规定
可采用硬质玻璃或聚乙烯容器采集水样,采样时用水样冲洗3次,再采集于容器中。
样品保存
样品采集后,(0~4)°C避光保存,12h内完成检测。
分析步骤
电极校准
按照仪器说明书选择校准模式,用pH标准缓冲溶液对电极进行三点校准,斜率在0.95~1.05 范围内。
滴定终点设定
按照仪器说明书的操作方法,设定第一个滴定终点的pH值为8.3,第二个滴定终点的pH值为4.4。
水样测定
取50.0 mL水样于测量杯中,测量杯置于滴定台上,插入电极和滴定头于水样液面之下,开启仪器和搅拌器,用盐酸标准滴定溶液自动滴定至反应结束。
实验数据处理
计算
碱性化合物在水中产生的碱度有五种情形,滴定至pH值为8.3时,消耗的盐酸标准滴定溶液体积记为P(mL),pH值从8.3降至4.4消耗的体积记为M(mL),滴定至pH值为4.4时消耗的总体积记为T(mL),水中碱度的组成在表1中给出。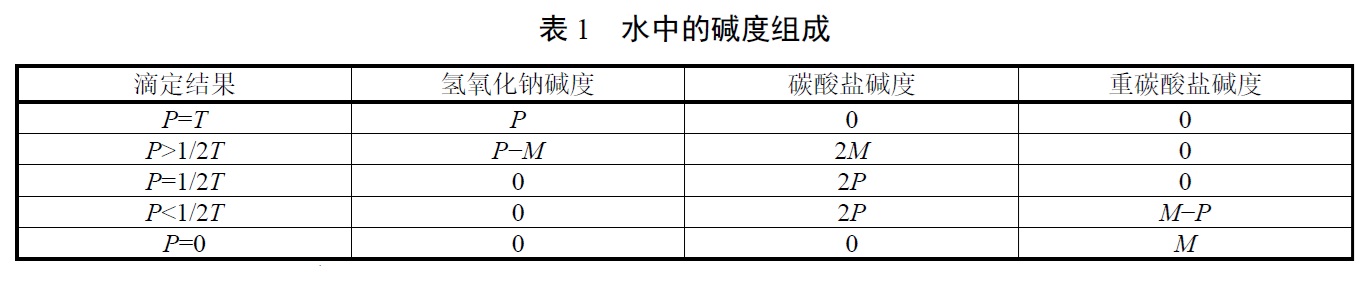
1) 当P=T时:![]()
式中:
A——水样的总碱度,以CaCO3计,单位为毫克每升(mg/L);
A1——氢氧化物碱度,以CaCO3计,单位为毫克每升(mg/L);
C——盐酸标准滴定溶液浓度,单位为摩尔每升(mol/L);
V——水样体积,单位为毫升(mL);
50.05——碳酸钙(1/2 CaCO3)的摩尔质量,单位为克每摩尔(g/mol);
1000——单位换算系数。
2) 当P>1/2T时: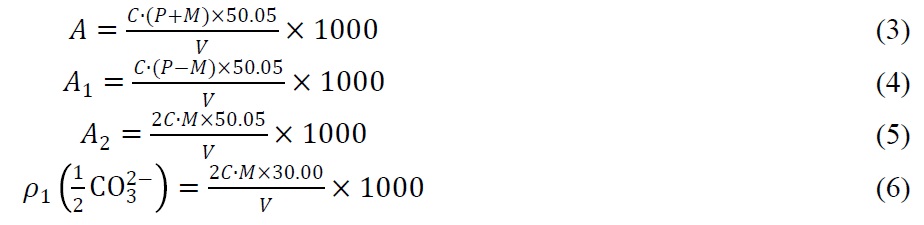
式中:
A2——碳酸盐碱度,以CaCO3计,单位为毫克每升(mg/L);
ρ1——碳酸盐的质量浓度,单位为毫克每升(mg/L);
30.00——碳酸根离子(1/2 CO32-)的摩尔质量,单位为克每摩尔(g/mol)。
3) 当P=1/2T时: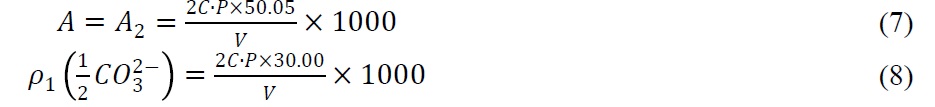
4) 当P<1/2T时: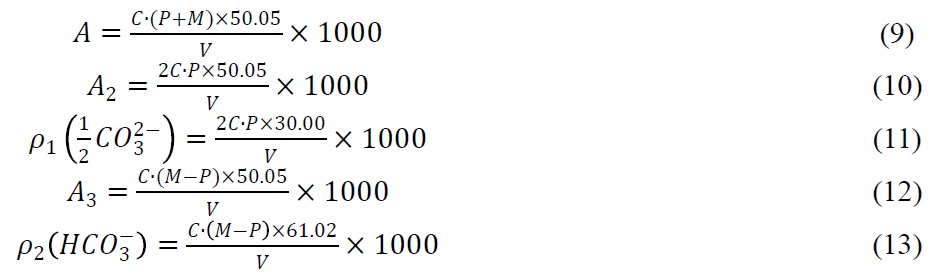
式中:
A3——重碳酸盐碱度,以CaCO3计,单位为毫克每升(mg/L);
ρ2——重碳酸盐的质量浓度,单位为毫克每升(mg/L);
61.02——重碳酸根离子(HCO3-)的摩尔质量,单位为克每摩尔(g/mol)。
5) 当P=0时:
结果表示
结果保留三位有效数字,小数不过两位,数值修约应按照 GB/T 8170 的规定执行。